Marcando presença até nos instrumentos musicais!
À primeira vista, parece haver pouca relação entre a química e os instrumentos musicais, o que só torna ainda mais divertido fazer um programa a provar exatamente o contrário!
Não interessa se são instrumentos de corda, de sopro ou de percussão, tanto a sua durabilidade como a qualidade do som que produzem dependem fortemente dos materiais que os constituem.
Um dos exemplos mais conhecidos da relação entre a qualidade do som e a química são os famosos violinos Stradivarius, considerados os melhores violinos de sempre. O seu som inimitável parece estar ligado ao tratamento químico da madeira e sobretudo às características do verniz utilizado no acabamento.

O polimento final dos instrumentos foi sempre uma ciência química, já que se baseia em tintas, vernizes e corantes. Mas é a moderna técnica de eletrodeposição que garante o melhor aspeto e qualidade de som dos instrumentos: permite recobrir as superfícies com finíssimas camadas de cobre, prata, ouro e níquel, em várias combinações, a partir de uma solução com ions destes metais e por aplicação de uma corrente elétrica que neutraliza a carga dos ions e força a sua deposição como sólidos.

Nos instrumentos de corda, a química volta a aparecer nas cordas! Até ao final do século 19, as cordas de guitarra eram feitas de bio polímeros obtidos a partir dos intestinos de animais: o “catgut” também utilizado em cirurgia.
Eram cordas difíceis de fazer, muito sensíveis à humidade e que facilmente desafinavam!
As cordas de polímeros sintéticos — como o nylon — surgiram como uma alternativa económica: são cordas resistentes à humidade e que não desafinam.
Mas as cordas mais apreciadas são as cordas metálicas, por produzirem um som muito claro e intenso. A sua estrutura — um fio metálico que se enrola em torno de outro — contribui para a boa qualidade sonora. O problema destas cordas é que os metais são sensíveis à corrosão, uma reação química muito facilitada pelo suor das mãos e que degrada a qualidade do som produzido.
Atualmente, a solução parece estar encontrada: proteger as cordas metálicas com uma finíssima cobertura de polímeros ou utilizar a química dos metais para produzir ligas metálicas resistentes à corrosão.
E assim temos a música e a química na mesma partitura, em perfeita harmonia!
A química do brigadeiro?!
Que tal preparar uma aula envolvendo a química presente no feitio de brigadeiro? Será uma oportunidade de relacionar conteúdo e prática de uma forma bem saborosa! Este contexto é referente à Estequiometria. Para uma melhor fixação da matéria, é recomendável que se assista à vídeo aula abaixo:
Para entender o conteúdo estequiométrico, é fundamental saber que transformações químicas acontecem numa proporção entre as substâncias que reagem, e essa proporção tem que estar correta.
Para fazer um bom brigadeiro precisamos obedecer a esse princípio químico, colocando a quantidade certa de cada ingrediente.Portanto, vamos aos ingredientes da sobremesa:
1 lata de leite condensado;
5 colheres (sopa) de chocolate em pó;
1 colher (sopa) de manteiga;

Modo de fazer: misture todos os ingredientes em uma panela e leve ao fogo brando até começar a desprender do fundo. Retire do fogo e despeje em um refratário untado. Está pronto seu brigadeiro, você pode enrolá-lo em forma de bolinhas ou comer na colher. Um bom exemplo de proporção foi dado na receita: para cada lata de leite condensado, cinco colheres de chocolate em pó e uma colher de manteiga... Por quê? Se você colocar menos chocolate seu brigadeiro ficará desbotado, se diminuir a quantidade de leite condensado terá uma sobremesa sem graça. E quanto à manteiga? Se não for a medida indicada (se for menos), seu brigadeiro ficará duro e quebradiço. Veja só, acabamos de envolver a Estequiometria na receita de brigadeiro! Podemos até escrever uma equação:
1 lata de leite condensado + 5 colheres de chocolate + 1 colher de manteiga → brigadeiro perfeito
Proporção 1 : 5 : 1.
Portanto, só teremos um brigadeiro perfeito se obedecermos à essa proporção estequiométrica.
Indicador de Repolho Roxo, uma forma natural da definição de pH!
Geralmente, os indicadores usados em laboratório são artificiais, tais como a fenolftaleína, o azul-de-bromotimol e o alaranjado-de-metila.
Mas, na natureza, também existem muitas substâncias que podem ser extraídas de espécies vegetais e que funcionam como indicadores ácido-base. O mais conhecido é o extrato de repolho roxo.
Para usar o repolho roxo como indicador ácido-base, basta você bater uma folha do vegetal com 1 litro de água no liquidificador e filtrar. Se você usar menos água para a mesma quantidade de repolho, obterá um indicador mais concentrado e de coloração mais intensa. Além disso, é bom guardá-lo em geladeira ou no congelador, porque ele se decompõe muito rápido.
Em água (pH neutro = 7), ele tem coloração roxa, mas conforme a imagem abaixo mostra, ele muda de vermelho em solução ácida para púrpura e depois verde, quando em solução básica. No caso da solução ser fortemente ácida, ele torna-se amarelo:
2- > 6, Acido;7-> Neutro; 8 ->. 11, Alcalino.

A formação dos elementos da origem do universo até os dias de hoje!
Nucleossíntese estelar: origens
É chamado de nucleossíntese o processo de formação dos elementos por um conjunto de reações nucleares que se dão no interior de estrelas, a elevadas condições de pressão e temperatura.
Entre 13 e 15 bilhões de anos atrás, segundo as mais atualizadas datações da idade do universo, houve uma grande explosão, chamada Teoria da Expansão ou do Big-Bang, criando o espaço e o tempo e liberando quantidade incríveis de energia, ao redor de 3 bilhões de graus célsius. A partir desse momento o Universo Primevo se encheu de radiação e partículas fundamentais chamadas de "quarks". A medida em que o Universo se expandia, e continua a se expandir até hoje, ele foi esfriando, permitindo que o quarks se unissem formando partículas de maior organização, como prótons, elétrons e nêutrons.
Assim foi criado o Hidrogênio, formado por apenas um próton e um nêutron em cada núcleo, é o elemento mais simples. Dentre os noventa e nove elementos, que ocorrem naturalmente, da tabela periódica o hidrogênio reivindica 99% dos átomos do cosmos. Com o contínuo declínio da temperatura no nosso jovem universo em expansão, formam-se bolsas de gás que ao chegar a mágica temperatura de 10 milhões de graus na escala absoluta, os prótons (que são simplesmente átomos de hidrogênio nus, privados de seus elétrons) se movem com rapidez suficiente para que ocorra a fusão nuclear do hidrogênio, convertendo-o em Hélio.
Este estágio, onde se formam o Hidrogênio e o Hélio, é chamado de Nucleossíntese Primordial e essas nuvens de gás são estrelas jovens em formação. A formação de todos os outros elementos mais pesados se dará no interior dessas estrelas.
.jpg?timestamp=1439498458530)
A gravidade:
Após a formação do Hélio e a diminuição da temperatura, as condições não são propícias para a reação e formação de novos elementos. O universo dá uma parada. Esta situação é chamada pelos estudiosos de "primeira crise do crescimento da complexidade", que dura cerca de um milhão de anos, até que o universo esfrie a uma temperatura que torne possível a formação de moléculas, que é o que acontece com o Hidrogênio. Eis aí a primeira molécula.
No universo primordial a radiação se sobrepunha a matéria, mas nessa nova fase com a formação de átomos e moléculas a matéria vai dominar os próximos acontecimentos. Com o predomínio da matéria sobre a radiação, surge a gravidade. não em níveis como conhecemos hoje, à escala universal, mas em níveis locais.
Para que uma estrela possa se formar é preciso que o gás e partículas presentes possam ser comprimidos, tornando a nuvem cada vez mais densa, levando-a a seu colapso gravitacionalmente induzido. Como o gás quente resiste mais à compressão que o gás frio, nos deparamos com uma situação estranha. É preciso que a nuvem esfrie antes que posso se aquecer e formar e a estrela. Uma estrela que possui um núcleo de 10 milhões de graus, quente o suficiente para da inicio à fusão termonuclear, requer que a nuvem atinja primeiro suas condições mais fria, apenas alguns graus acima do zero absoluto. Que é precisamente o que acontece no período da chamada "crise de crescimento da complexidade".
Durante esse período, pedaços maiores de matéria (moléculas) atraem os outros, aumentando a densidade da nuvem e durante esse processo a contração converte a energia gravitacional das bolsas de gás em calor. A temperatura dentro de cada uma dessas regiões eleva-se rapidamente, até atingir o valor crucial para a fusão termonuclear.
Após atingir a temperatura adequada, além da fusão do Hidrogênio em Hélio, ocorre a formação do Carbono. A combustão do carbono, relativamente complexa, produz vários elementos como o néon, o sódio, o magnésio, o alumínio, o silício e, em menor quantidade, o fósforo e o enxofre. É dessa fusão que a estrela retira sua energia, parte da massa dos núcleos fundidos é perdida e transformada, num equilíbrio descrito pela equação de Einstein (a energia é igual a massa multiplicada pela velocidade da luz ao quadrado) que é liberado em forma de luz (fótons) e calor, como o nosso sol. A partir do mesmo processo, a estrela, agora extremamente quente e densa, continua a formar elementos, cada vez mais complexos, para se sustentar, até que é formado o ferro, que tem a mais alta energia de ligação por partícula nuclear e para que seja realizada sua fissão é necessário abastece-lo com energia adicional, isso quer dizer que a estrela esgotou todas as suas opção de liberação de energia por fusão nuclear, levando a estrelar a colapsar.

Supernova:
Todos já ouvimos a famosa frase do astrônomo Carl Sagan que diz: "somos feitos do pó de estrelas". A maior parte das pessoas não leva tal afirmação no sentido literal, assim como eu não levava, mas, por mais louco e abstrato que pareça, é verdade.
Após a formação do Ferro, quando a estrela esgota suas fontes de energia, ela sucumbe a sua própria gravidade, primeiro aumento absurdamente de tamanho e depois se contraindo, até que explode liberando quantidades inimagináveis de energia e espalhando pelo cosmos todos os elementos que conhecemos hoje, formados dentro das estrelas. É a partir desses elementos que irão se formar os planetas, outras estrelas, nebulosas e galáxias.
Ou seja, o Carbono, que está presentes em tudo a nossa volta, inclusive nos nossos corpos, o gás Hélio, que usamos em balões e aspiramos para afinar a voz, o Oxigênio, essencial para a vida, o Fósforo, o Ferro e o Alumínio presentes no nosso dia-a-dia, todos e tudo fizeram parte, um dia, de uma estrela. E esses compostos se comportam de formas distintas e as vezes imprevisíveis, como o Cloro, que puro é um gás fedorento e mortal, mas combinado com o sódio, temos o sal de cozinha, inofensivo. E o Hidrogênio e o Oxigênio, dois dos elementos mais abundantes do universo? Um dele é um gás explosivo e o outro promove uma violenta combustão, mas os dois juntos formam a água líquida que apaga o fogo. Intrigante essa tal de química, não?

Fontes:
- Neil deGrasse Tyson e Donald Goldsmith - "Origens". Ed Planeta
- Margaret Burbigde, Geoffrey Burbigde, Fowler e Hoyle - "Reviwes os Modern Physics"
- Wikipédia - Nucleossíntese
- Wikipédia - Reação Nuclear, Fusão e Fissão
A química nos celulares!
Elas podem ser chamadas de baterias de íon-lítio. Possuem esse termo por ser o lítio a sua matéria prima básica na qual é capaz de produzir 2x mais energia do que as baterias de zinco-carbono ou alcalina. Também geram uma duração maior de 3 volts.

Seu funcionamento é basicamente permitir o fluxo de elétrons negativos seja convertido para positivo, desse jeito a energia é direcionada para a estrutura de lítio. Hoje em dia existe 4 principais tipos de bateria: íon-lítio, níquel híbrido, lítio polímero e níquel-cádmio. Segundo estudo a bateria mais segura de explosões e as mais rentáveis são as de íon-lítio por serem mais viáveis, além do tempo de recarga mais rápido.
Elas são compostas por células de íon, que podem ser encontrados nos formados piramidal ou cilíndrica, além de possuírem sensores de temperaturas (para alertar se o nível da bateria está muito grande ou não) Cabo conector, conversor de tensão e circuito regulador de tensão. O funcionamento da bateria pode ser melhor compreendido com o conhecimento da pilha de Danniel assistindo a vídeo aula abaixo:
A Coca Cola realmente desentope pias?
Refrigerantes são água carbonatada ( na qual se dissolveu gás carbônico) e substâncias químicas para dar cor e sabor, que provocam sensação agradável quando ingeridos. Em geral, os refrigerantes são compostos de substâncias químicas sintéticas. Bebidas com sabor laranja usam uma pequena fração de suco de laranja. Não usam mais porque o suco natural tem maior tendência à decomposição.

Agora, desentupir pias, a Coca-Cola não desentope, contrariando dito popular. A Coca-Cola é um derivado de um extrato vegetal de composição variável, ao qual é adicionado ácido fosfórico em pequena quantidade, como conservante. A confusão se dá porque esse ácido é usado por fabricantes de material de limpeza, mas não faz mal ao ser humano.
Nas reações químicas que ocorrem nas células, várias delas usam o fosfato, que é um componente do ácido fosfórico. A célula usa o fosfato (PO4-3) no mecanismo de fornecimento de energia celular. Mas há uma ressalva: o excesso de fosfato pode reagir com o cálcio (Ca+2), componente de ossos e dentes, e causar problemas ósseos ou dentários. Nada além disso.
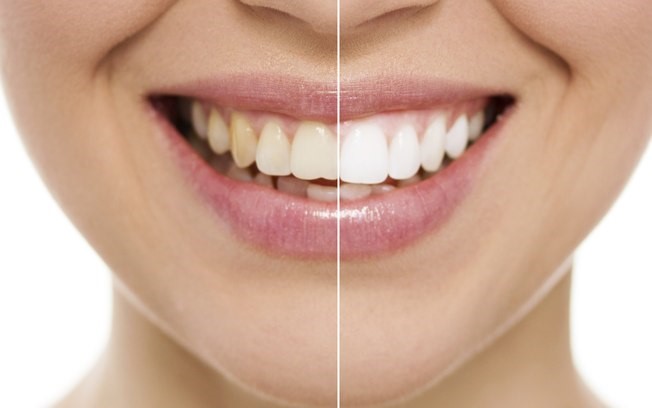
Como clarear seus dentes em 4 passos com a química!
1- Misture o bicarbonato de sódio com água: Em uma pequena xícara, misture meia colher de chá de bicarbonato de sódio com meia colher de chá de água. Misture para formar uma pasta;
2- Escove os dentes de um a dois minutos: Escove os dentes como você normalmente faria, mas concentre-se em passar a escova em todas as aberturas e reentrâncias. Não escove os dentes por mais de dois minutos, já que o bicarbonato de sódio é um abrasivo leve e pode começar a corroer o esmalte dos seus dentes;
3- Enxágue: Cuspa o bicarbonato de sódio e enxágue a boca com água ou enxaguante bucal. Lave bem a sua escova de dentes também;
4- Repita em dias alternados: Você deve repetir o processo de escovação dos dentes com bicarbonato de sódio em dias alternados de uma a duas semanas. Você irá perceber uma leve diferença entre a cor dos seus dentes depois de alguns dias e uma diferença substancial depois de duas semanas.
Depois de duas semanas escovando os dentes com bicarbonato de sódio em dias alternados, você diminuir a frequência para apenas uma ou duas vezes por semana. Isso é porque as propriedades abrasivas do bicarbonato de sódio podem danificar o esmalte dos seus dentes se o bicarbonato for usado com muita frequência.
*Esteja ciente de que escovar seus dentes com bicarbonato de sódio não deve substituir a escovação com a pasta de dente. A pasta de dente contém flúor, que é importante para fortalecer os dentes e prevenir cáries.*
Por que esse processo funciona? Isso ocorre pois o bicarbonato é uma substância abrasiva, que funciona como um esfoliante no esmalte dentário e remove a placa bacteriana, sujeira e até algumas manchas, dando a sensação de que o dente ficou mais branco – quando, na verdade, ele está apenas mais limpo. Por outro lado, o produto desgasta o esmalte do dente, deixando-o mais exposto à infecções e causando sensibilidade.
Bicarbonato de sódio, aonde e como usar?
O bicarbonato de sódio é útil em quase tudo. Pode ser usado umas pitadas em cima do creme dental, ajuda a branquear os dentes. Usa-se uma colher (cafezinho) em ½ copo de água para fazer bochecho após escovar os dentes, ajuda a combater à carie dentária e aftas. Quando sai firidinha no canto da boca ou na língua, coloca-se uma pitada em cima, arde e queima um pouquinho, mas logo cura, aplicar 3xdia. Usa-se também em bolos junto do fermento bem pouquinho para massa ficar leve. Usa-se como antiácido para aliviar dor de estomago. Usa-se com água morna uma colher (sopa) bem cheia em meio litro de água, para limpar a geladeira, tira o odor impregnado de alimentos. E também tem várias dicas de limpeza onde é utilizado o bicarbonato de sódio. Enfim, se faz várias coisas com bicarbonato de sódio, por isto é importante sempre ter em casa.

►Como antiácido para aliviar dor de estomago: Dissolver 2,5g (1 colher de café) em um copo de água filtrada e tomar 30 minutos antes das refeições, para neutralizar o excesso de secreção gástrica no estômago. Não usar juntamente com dieta láctea (a base de leite) devido a possibilidade de ocorrência de síndrome alcalino-láctea. (Fonte: Resolução-RDC N° 199, de 26 de outubro de 2006 – ANVISA)
►Remoção de odores de geladeira e freezer: Depois de retirado todo o gelo, limpe com um pano limpo ligeiramente embebido em água com bicarbonato de sódio [uma colher (sopa) bem cheia em meio litro de água morna] e depois seque com um pano limpo. Esta mesma solução pode ser utilizada para retirar qualquer cheiro forte que tenha ficado no plástico, mergulhe os vasilhames em água com bicarbonato de sódio, e deixe por vários minutos, depois lave normalmente com água.
►Limpeza da cafeteira de aço inox: Adicione duas colheres (sopa) de bicarbonato de sódio a um volume de água equivalente a sua capacidade, deixe-a ferver durante 10 a 15 minutos numa vasilha e então despeje a solução sobre a cafeteira.
►Limpeza da garrafa térmica: Lave a ampola (vidro prateado) com uma solução de água quente e bicarbonato de sódio para retirar resíduos do líquido. Enxágüe bem. Não use utensílios de metal para limpar a ampola de vidro, pois ela é frágil.
►Sujeira ou manchas no aço: Aplique uma mistura feita com bicarbonato de sódio dissolvido com álcool etílico, até formar uma pasta (tipo pasta cristal), usando um pano macio ou uma bucha de náilon para passar na superfície do aço inox, faça-o sempre da maneira mais suave possível, utilizando passadas longas e uniformes, no sentido do acabamento polido, caso houver. Evite esfregar com movimentos circulares, depois, enxágüe com bastante água, preferencialmente morna e seque com pano macio.
►Use bicarbonato de sódio na limpeza de utensílios de inox, dissolva 1 colher (sopa) de bicarbonato de sódio em um litro de água e lave as peças.
►Para limpar panela queimada, salpique com bicarbonato de sódio e umedeça, depois de algumas horas lave, o queimado sairá facilmente. E, se a comida grudou, encha a panela com água quente e duas colheres de bicarbonato de sódio. Deixe algum tempo e limpe.
►Para cinza de cigarro no cinzeiro que continuam a queimar e são desagradáveis, evite isso colocando um pouco de bicarbonato de sódio no fundo do cinzeiro.
►Limpeza de carpetes: Uma desodorização rápida pode ser obtida pulverizando-se o carpete com bicarbonato de sódio e aspirando logo a seguir.Para evitar manchas amareladas em lycra branca: depois de lavar e enxaguar, logo em seguida, deixar por pouco tempo de molho em água contendo um pouco de bicarbonato de sódio, secar a sombra.
►Para tirar aquelas marcas que com o uso ficam nas bordas internas das xícaras de café ou chá, basta esfregar bem com um pano úmido e bicarbonato de sódio.
►Para desentupir o cano da pia, jogue dentro dele um pouco de bicarbonato (2 a 4 colheres de sopa), derramando em seguida meia xícara de vinagre. ►Para limpar pentes, escovas e rolos de cabelo: Adicione 3 colheres (sopa) de bicarbonato de sódio em ½ colher (sopa) de hipoclorito de sódio numa bacia com um pouco de água morna. Coloque os objetos e deixe um pouco, mexendo sempre. Enxágue e deixe secar no ar.
►Para remover o mofo das cortinas do chuveiro: Use bicarbonato de sódio.
►Para remover a corrosão da bateria: Esfregue os terminais da bateria e ganchos com uma solução de água com bicarbonato de sódio. Depois passe vaselina sólida.
►Ladrilhos e cerâmicas: Para uma limpeza leve, lave os ladrilhos com uma solução de ½ xícara de amônia, ½ xícara de vinagre branco, ¼ de xícara de bicarbonato de sódio em 1 litro de água morna.
►Para tirar manchas de ferrugem nos tecidos, passe uma mistura de suco de limão com bicarbonato de sódio. Ou coloque suco de limão sobre a mancha, depois cubra o local com sal e deixe no sol por 20 minutos. Para ambos os casos, repita a operação se a mancha persistir e depois lave normalmente. Para remover as manchas de ferrugem em tecidos pode ser utilizado também o Tira Ferrugem.
►Manchas amareladas de tecidos: Para clarear tecidos de algodão e linho já amarelados pelo tempo, ferva o tecido numa panela bem limpa por 1hora em uma solução de sal de cozinha e bicarbonato de sódio.
Bicarbonato de Sódio:
O bicarbonato de sódio (NaHCO3) é um antiácido estomacal, pois neutraliza o excesso de ácido clorídrico (HCl) no suco gástrico. NaHCO3 + HCl → NaCl + H2O + CO2 É o principal componente do sal de frutas, que contém ainda ácidos orgânicos sólidos, como o ácido tartárico, o ácido cítrico e outros. A efervescência do sal de frutas se deve a liberação do gás carbônico (CO2). Na higienização bucal, na forma de bochecho o bicarbonato de sódio atua na neutralização dos ácidos que atacam o esmalte dentário, também para o combate de aftas. Também é utilizado na fabricação de fermento para pães, bolos, biscoitos, etc. Quando o bicarbonato de sódio é aquecido, há liberação do gás carbônico (CO2), que faz a massa crescer. 2NaHCO3 → Na2CO3 + H2O + CO2. Pode também ser usado na fabricação de extintores de espuma, que possuem em compartimentos separado, bicarbonato de sódio (NaHCO3) e ácido sulfúrico (H2SO4). Quando o extintor é acionado, o NaHCO3 mistura-se com o H2SO4 e essa reação produz CO2, que apaga o fogo. Esses extintores não são utilizados para apagar o fogo em instalações elétricas, porque a espuma é eletrolítica (conduz corrente elétrica). O Bicarbonato de sódio é utilizado no tratamento de água para piscinas como controlador de pH (agente tamponante).
Algumas Propriedades:
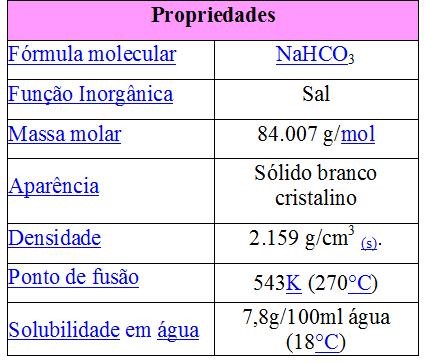
Observação: Apesar de apresentar hidrogênio na sua estrutura (NaHCO3), ele não é classificado como um sal ácido e sim como um HIDROGENOSSAL, devida a presença do hidrogênio. Este sal quando adicionado na água, mostra por sua hidrólise salina (reação de um sal com á água) que o mesmo apresenta características básicas (pH >7), por ser um sal proveniente de uma base forte (NaOH) e de um ácido fraco (H2CO3).
Os vários usos da cerveja!
Muita gente acha que cerveja serve apenas para beber, mas esse líquido tem muitas outras utilidades que as pessoas nem imaginam. Se você está com pena de jogar aquela cerveja fora, seja por estar vencida ou perdeu o gás, veja algumas aplicações que podem mudar seu dia.
Condicionador de Cabelos: Cabelos secos e sem vida, amiga? Seus problemas acabaram! Depois de lavar seus cabelos com seu xampu, aplique uma generosa quantidade de cerveja sem gás e deixe alguns minutos. Após enxaguar, você estará deslumbrante! A cerveja é rica em vitamina B, graças as leveduras, que adicionam corpo e brilho aos cabelos;

Marinar carnes e cogumelos: Quem gosta de cozinhar ja deve ter conhecimento dessa. Faça pequenos furos na carne e deixe passar a noite descansando em uma mistura de cerveja com temperos. A acidez da bebida ajuda a deixar a carne mais tenra;

Polir metais: Quem já visitou uma cervejaria que usa os tradicionais panelões de cobre viu como eles estão sempre brilhando. Isso acontece porque a acidez da cerveja ajuda a polir alguns metais. Molhe uma toalha com cerveja e esfregue naquela panela velha de casa. É menos agressiva a saúde que polidores de metais tradicionais!;

Tijolos para construção civil!: Na origem da fábrica algumas garrafas de cerveja eram quadradas, pois os donos queriam ajudar as pessoas que compravam a cerveja a construir suas casa. Empilhando diversas garrafas, é possível construir paredes ecológicas que permitem que a luminosidade do dia ajude a clarear o ambiente, diminuindo a necessidade de luz ambiente;

A verdade por trás da pergunta: qual shampoo limpa mais: o que produz espuma ou o que produz menos espuma?
Existem diversas duvidas que passamos no nosso cotidiano. Uma delas ocorre muitas vezes durante o banho, será que o shampoo que faz mais espuma limpa mais do que o que produz menos? A resposta é não, isso é apenas um mito da sociedade. Pois principal matéria-prima de um shampoo é o tensoativo. Ele tem a capacidade de se agarrar simultaneamente à água e à sujidade oleosa. Com isto arrastra a sujeira junto com a água para o ralo do chuveiro. Quando o tensoativo não tem sujidade oleosa para se ligar, ele acaba se ligando com o ar e forma uma bolha de sabão (a espuma). Sendo assim apenas quando não tiver mais sujeira é que começa a se formar uma espuma mais abundante. Ao contrário de que muitos pensam, o shampoo que é mais recomendado por dermatologista são os que são os livres de sulfato em sua composição, pois o shampoo sem sulfato é mais suave e faz pouca ou nenhuma espuma, eles também higienizam o cabelo sem esfregações ou espuma. Basta uma massagem suave em todo couro cabeludo e, em seguida, enxaguar. É uma forma de manter as cutículas intactas, e é uma excelente opção para cabelos porosos ou danificados. Mas então pensamos será que o shampoo sem sulfato seria o mais recomendado para todos os tipos de cabelo? Os shampoos sem sulfato são mais indicados para que tipos de cabelos? Para cabelos crespos, com químicas, cacheados, finos, frágeis, tingidos e descoloridos. Esses shampoos ajudam a deixar os cachos mais soltinhos, definidos e sem frizz. Aumentam a durabilidade da coloração, diminuem o atrito entre os fios e até mesmo reações alérgicas. Para quem tem fios ou couro sensíveis esse tipo de shampoo também é uma ótima opção: ele mantém as cutículas preservadas, diferentemente dos shampoos sintéticos.

Os principais benefícios do shampoo sem sulfato:
- Ajuda a manter a cor dos cabelos mais vivas, evitando o desbotamento rápido;
- Evita alergias no couro cabeludo;
- Evita a quebra capilar, a porosidade e o ressecamento;
- Ajuda a fibra capilar a ficar mais resistente e saudável;
Demaquilantes,afinal,o que são?
Muito se fala sobre usar maquiagem, mas muito pouco sobre tirar a maquiagem. A pele é composta por tecidos, glândulas sebáceas e folículos. Vários especialistas defendem que alguns compostos químicos (sintéticos, corantes, conservantes, pó de talco mineral, etc…) presentes na maquiagem podem acarretar o entupimento dos poros. A pele não “respira” naturalmente quando é revestida com maquiagem. Essa obstrução dos poros pode favorecer o aparecimento de acnes, cravos, o aumento da oleosidade da pele e acarretar outros problemas mais sérios. Em alguns casos, a combinação: poros entupidos, acnes e sol pode até provocar mancha.

Os demaquilantes são apolares. Eles são produtos desenvolvidos para removerem a maquiagem da área dos olhos, boca e pele. Devido ao seu contato direto com os olhos sua formulação se diferencia dos higienizadores em geral. Existem dois tipos de demaquilantes, os destinados para maquiagem hidrossolúveis (solúveis em água) como o pó facial, compacto, sombra em pó etc. e para maquiagem à prova d’água (water proof) como algumas máscaras, batons, blushs em bastão, sombra em bastão etc., que devido à sua composição são muito mais difíceis de retirar. Demaquilantes hidrossolúveis são encontrados geralmente sob forma de loções aquosas ou de géis aquosos (loções gelificadas) compostos ou não de tensoativos suaves. Esses produtos devem ter um pH próximo ao das lágrimas (7,5) e serem isotônicos a fim de não provocar irritação. Eles diluem rapidamente a maquiagem das pálpebras e máscaras de cílios comuns, mas não são muito utilizados quando a quantidade de maquiagem é maior ou existe a presença de materiais graxos. Demaquilantes para maquiagem do tipo water proof são compostos basicamente por óleo ou cremes do tipo (possuem mais óleo do que água). Normalmente devem ser aplicados na pele com massagens suaves, para assim incorporar na fase oleosa as gorduras da pele e matérias graxas da maquiagem, bem como as sujidades hidrossolúveis na fase aquosa, em seguida faz-se a remoção com algodão ou lenço de papel. É necessário proceder com o enxague com água ou tônico adequado, para completar a limpeza. Ainda existem os demaquilantes à base de silicone, que faz a remoção da sujidade graxa sem deixar vestígio oleoso na pele. Esse tipo de maquiagem muitas vezes nem precisam de enxague.